

Un kit pour identifier les goûts de souris
Depuis 2017, le goût de souris fait l’objet de remontées de terrain, problématique récurrente, dont l’apparition est favorisée par des conditions de milieu plus favorables qu’auparavant : moins de sulfitage, des ph globalement plus élevés et augmentation du recours à la flore indigène. Il est considéré aujourd’hui par les professionnels comme un défaut altérant la qualité organoleptique des vins. Un sondage lancé courant 2019, par l’IFV Centre Val de Loire montre qu’environ 40 % des viticulteurs ne savent pas reconnaître cette altération organoleptique et près de 80 % sont intéressés pour être formé à sa reconnaissance démontrant l’opportunité de proposer une action de formation spécifique.
L’un des objectifs des rendez- vous techniciens du 21 et 22 juin dernier, organisé par InterLoire en collaboration avec l’IFV Centre Val de Loire a donc été de former les techniciens du Val de Loire, œnologues-conseil, responsables techniques, maitres de chai, à la reconnaissance du goût de souris au travers d’une dégustation de vins sourissés et d’une présentation d’un kit pédagogique de reconnaissance crée par L’unité IFV de Vertou.
Un coffret pédagogique pour faciliter sa reconnaissance
Cet outil, en format « coffret », est composé de trois vins à défaut : un chenin, un assemblage de chenin et cabernet ainsi qu’un gamay. On n’y trouve également un échantillon d’arôme de pandan (plante tropicale utilisée dans la cuisine en Asie du sud-est et dont la saveur des feuilles évoque l’odeur de popcorn, une des composantes du goût de souris), du bicarbonate de soude en poudre et des bandelettes imbibées de soude. Le bicarbonate de soude ajouté à l’échantillon de vin à raison d’environ 5 g/l permet de remonter le pH de l’échantillon aux environs de 5. Ceci rendant plus facile la perception en bouche (via la voie rétro-nasale) des pyridines, molécules responsable du goût de souris. Les bandelettes préalablement trempées dans le vin permettent quant à elles une détection olfactive et la dégustation de plusieurs échantillons sans phénomène de saturation. Ce kit pédagogique est disponible sur demande auprès de l’IFV pôle Centre Val de Loire (contactez Marie-Charlotte Colosio ou Emy Heguiaphal). Outre la présentation de l’outil, Nicolas Richard, Œnologue au service R&D d’Inter Rhône, un des intervenants de la journée, a fait bénéficier les participants de son expérience en la matière. Il conseille notamment, lors d’une dégustation de plusieurs échantillons, de bien se rincer la bouche avec de l’eau entre chaque échantillon et d’être vigilant sur la perception gustative tout au long de la dégustation. Cette précaution tient compte du fait de la variation du pH buccal dans la journée et de la variation de l’intensité du goût de souris dans un vin tenu à l’air.
Origine du goût de souris et solutions
En introduction, les intervenants ont explicité qu’elles étaient les origines probables du développement des goûts de souris et les solutions possibles pour y remédier. Deux mécanismes possibles sont mis en avant par les scientifiques. Les pyridines peuvent être produites par la voie microbiologique, via Brettanomyces et les bactéries lactiques (oenococcus oeni, lactobacillus, pediococcus). Il semblerait qu’elles soient produites également par voie chimique en présence d’éthanal, de sucres et d’acides aminés ; ces réactions chimiques complexes étant favorisées par l’augmentation de la température et du pH et fonction de l’équilibre oxydo-réducteur du vin. Leur apparition est souvent liée à d’autres défauts (oxydation, défauts olfactifs liés au développement de Brettanomyces). Les expérimentations réalisées dans le cadre du projet ont montré qu’il fallait plutôt travailler en préventif qu’en curatif. Les essais d’ajout de différents produits œnologiques n’ont pas mis en évidence de solutions miracles. Beaucoup de questions relatives aux facteurs et mécanismes de déclenchement de l’apparition du défaut sont donc encore en suspens et nécessitent une poursuite des travaux.
Pour en savoir plus :
Consultez aussi Tous les articles


Les clés d’une bonne conservation des vins rouges
Compte tenu des aléas climatiques récurrents, la maîtrise des stocks tant d’un point de vue qualitatif que quantitatif s’avère aujourd’hui un enjeu majeur pour le pilotage d’un vignoble. Le syndicat des vins de Chinon a ainsi saisi l’opportunité le 6 septembre dernier, dans le cadre de sa journée technique pré-vendanges, d’aborder la thématique du stockage et la conservation des caractéristiques organoleptiques, dans les vins rouges en vrac.
La flore microbienne présente dans les moûts et dans les vins est constituée principalement de levures, fermentaires et non fermentaires et de bactéries lactiques et acétiques. En fermentation alcoolique, se développeront majoritairement des levures dites fermentaires transformant les sucres en alcool, genre saccharomyces cerevisiae. En fermentation malo-lactique, ce sont des bactéries lactiques (oenococcus, lactobacillus plantarum, pediococcus), majoritairement, qui métaboliseront l’acide malique en acide lactique. Au cours de l’élevage, pendant la phase de stockage et jusqu’en bouteille, différentes populations, résistantes à l’alcool et au SO2, capable de vivre en état de stress, dans des milieux pauvres en nutriments, favorisées par des conditions d’environnement plus favorables (température, ph élevé), seront susceptibles de proliférer et d’induire diverses altérations modifiant le profil aromatique et gustatif du vin. On peut citer brettanomyces (levures) productrices de phénols volatils, candida (levures) responsables de la maladie de la fleur (formation d’un voile de surface), des bactéries acétiques (aérobies) genre acétobacter ou gluconobacter responsables de piqûre acétique (production d’acide acétique et d’acétate d’éthyle). Les bactéries lactiques peuvent également, si elles dégradent des sucres, provoquer une piqûre lactique.
Un suivi de cette flore indispensable
Lors de son intervention, Marie-Charlotte Colosio de l’IFV pôle Val de Loire-Centre a insisté sur le goût de souris, présent de manière récurrente dans certains vins, du fait d’une moindre utilisation de SO2 avec des Ph toujours plus élevés. « Il apparaît en cours d’élevage et de stockage, après les fermentations ; il est perceptible uniquement en bouche en rétro-olfaction, quand le Ph du vin augmente au contact de la salive avec des seuils de perception variables en fonction de l’individu. Il peut être produit par des bactéries lactiques et des levures d’altération comme brettanomyces », rappelle-t-elle. Pour prévenir toute déviation, Marie-Charlotte Colosio conseille un suivi de la population microbienne en cours d’élevage et de stockage, l’observation de bonnes pratiques œnologiques pour éviter les contaminations initiales (maîtrise des températures, teneur en SO2 suffisante, hygiène du chai et des matériels) et des interventions de manière préventive. « Nous constatons souvent l’altération tardivement, à postériori, à la dégustation », remarque-t-elle. En actions correctives, l’utilisation de lysozyme, permettant une diminution de la population de bactéries lactiques, de Chitosane dans le cas de développement de brettanomyces, peuvent être des alternatives efficaces comme la flash-pasteurisation et la filtration, complète Marie-Charlotte Colosio.
Attention à l’oxygène dissous
Tout au long du stockage d’un vin en vrac, deux éléments-clés seront déterminants et nécessaires de maîtriser pour une bonne conservation : l’oxygène et sa capacité à être solubilisé et consommé et la teneur en SO2. L’oxygène, au contact du vin se solubilise jusqu’à saturation - on parle d’oxygène dissous, seule forme capable d’être dosée dans le vin - puis est consommé. Les basses températures en cours de manipulation, les phénomènes d’émulsion en cuve et au niveau des pompes à vin lors des transferts, l’augmentation de la surface de contact entre l’air et le vin en cuve seront des facteurs facilitant sa dissolution. En phase statique, les températures élevées (>17°c), favoriseront une consommation plus rapide de l’oxygène dissous. La présence de polyphénols et de lies de levures en le métabolisant protègeront quant à eux d’autres constituants du vin (matières colorantes et arômes). « Pratiquement, il serait souhaitable de maintenir une température de stockage entre 8 et 12°c en hiver, idéalement entre 12 et 15°c (hors périodes hivernales), privilégier une température >13°c lors de manipulations, en limitant les vitesses de pompage notamment en fin et en début d’opération et la longueur des tuyaux », précise Pascal Poupault de l’IFV pôle Val de Loire-Centre.
Optimiser la gestion du SO2
Le SO2, utilisé à bon escient, grâce à ses propriétés, protège le vin contre l’oxydation (1mg /l d’O2 dissous oxyde 1 à 4 mg/l de SO2) préservant ainsi couleur et arômes. Il protège également le vin des déviations microbiennes (propriété antiseptique du SO2). Il revêt deux formes : le SO2 combiné peu efficace et le SO2 libre dont une fraction, le SO2 actif ou moléculaire représente la part la plus active. La proportion de cette dernière fraction est variable en fonction du ph, du degré et de la température. Une application proposée par l’IFV Occitanie permet de la calculer et d’ajuster précisément un sulfitage, en fonction du niveau de protection souhaitée. De manière générale, Pascal Poupault recommande de maintenir une teneur suffisante en SO2 libre en cours de stockage de l’ordre de 25 mg/l, de rajouter l’équivalent d’1 g/hl lors de transfert, tout en respectant les teneurs maximales légales.
Inerter les cuves en vidange et lors des transferts
L’inertage permet de limiter la dissolution de l’oxygène dans le vin lors du stockage et des transferts. Il consiste à injecter un gaz inerte azote ou CO2 au niveau des ciels de cuve en vidange, des tuyaux et cuves de réception. L’azote est le gaz le plus utilisé en œnologie. Il a l’avantage d’être plus économique et se dissout peu à contrario du CO2 qui petit à petit se solubilise dans le vin. Par contre dissous dans le vin, le CO2 réduit la vitesse de dissolution de l’oxygène. « Il est important de maintenir un niveau de SO2 libre suffisant et une température stable et fraîche pour prolonger la stabilité organoleptique des vins rouges stockés en vrac. Le collage, une teneur en CO2 élevée peuvent aussi contribuer à préserver la fraîcheur des vins » souligne Pascal Poupault. Après un échange avec la salle, Laure CAYLA de l’IFV Nouvelle Aquitaine, en conclusion de cette matinée, mis l’accent sur l’intérêt de mettre en place un suivi microbien des vins stockés afin d’anticiper les problèmes et d’identifier en amont l’aptitude des cuvées à se conserver en fonction de leur caractéristique organoleptique notamment leur teneur en polyphénols (tannins).
Pour en savoir plus,
-
Les interventions de Marie-Charlotte Colosio et Pascal Poupault
-
Les fiches techniques :
Consultez aussi Tous les articles


Le ou les goût(s) de souris, une altération loin d’être comprise
Les premières descriptions du goût de souris datent de la fin du XIX siècle. Cette altération d’origine microbienne est observée sur les vins blancs, rosés, rouges, tranquilles ou effervescents depuis longtemps mais une recrudescence de ce défaut est constatée depuis deux ans. Cette augmentation est à mettre en lien avec la diminution des doses de SO2, la hausse du pH des vins voire le recours aux flores indigènes. Patricia Ballestra de l’ISVV de Bordeaux a fait le point lors de la matinée technique de l’IOC en juin dernier à Chinon et du colloque régional de la Chambre d’agriculture du Loir-et-Cher en juillet.
Urine de souris, pop-corn, riz soufflé, peau de saucisson, serpillère, vomi,…. Sont autant de descripteurs utilisés pour caractériser le goût de souris. Peut-on alors parler des goûts de souris ? La diversité des descripteurs vient du fait que plusieurs molécules sont impliquées dans la formation de cette déviation. A ce jour, trois molécules N-hétéocycles ont été identifiées : la 2-ethyltetrahydropyridine (ETHP), la 2-acetyltetrahydropyridine (ATHP) et la 2-acetyl-1-pyrroline (APY). En cas de goût de souris, au moins 2 de ces 3 molécules sont présentes.
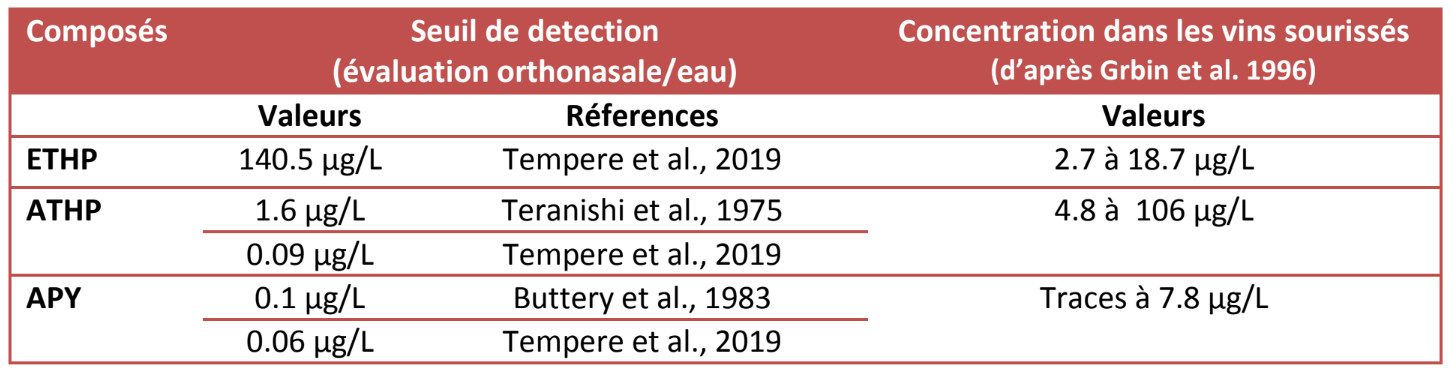
Source : P. Ballestra – ISVV Bordeaux
L’impact de la concentration à laquelle ces molécules sont présentes, l’effet matrice du vin mais surtout la différence de seuil de perception des individus jouent également sur les différences ressenties. Par exemple, le seuil de perception de l’APY, peut varier d’un facteur 100 d’un individu à l’autre.
La perception dépend du pH de la salive
L’ETHP, l’ATHP et l’APY ne sont pas suffisamment volatiles au pH du vin pour être perçues en olfaction car elles sont sous forme aminée. En revanche une fois le vin mélangé à la salive, dont le pH entre 5,76 et 7,96 favorise la forme iminée des molécules, le goût de souris est percevable et même persistant en retro-olfaction. La différence de perception est donc fonction du pH buccale qui varie selon chaque individu voire, pour chacun, selon le moment de la journée et l’état physiologique. Cette différence est à l’origine du manque de consensus entre les dégustateurs permettant d’identifier et d’évaluer l’intensité du goût de souris. Pour s’affranchir de ce frein, des préconisations ont été testées par l’ISVV, l’IFV et Inter-Rhône sur vin rouge. Il en résulte que l’alcanisation du vin en augmentant son pH à environ 5 à l’aide de 5g/l de bicarbonate de soude permet la détection et la discrimination du goût de souris par voie olfactive. Reste à tester cette méthode sur vin blanc et rosé.
Des mécanismes de formation encore à l’étude
Nous savons que le goût de souris est d’origine microbienne : la levure brettanomyces et les bactéries lactiques lactobacillus, Oenococcus et Pediococcus peuvent produire de l’ATHP, de l’ETHP, et de l’APY. En revanche, la voie de formation de ces molécules n’est, à ce jour, qu’hypothétique. Il est constaté le rôle de l’acétaldéhyde, de l’éthanol et de certains ions dans la formation de l’ATHP et l’APY alors que L’ETHP serait issue de la réduction de l’ATHP. Deux acides aminés présents naturellement dans le vin sembleraient être des précurseurs de l’ATHP et de l’APY: le L-lyzine et le L-ornithine. Mais la présence de ces derniers dans le vin pose la question suivante : pourquoi certains vins ont un goût de souris et pas d’autres ? Est-ce lié au métabolisme microbien ? A la concentration en tanins, en précurseurs ou en acétaldéhyde en donc en SO2 ? Autant d’hypothèses qui seront travaillées dans une thèse qui démarrera à la rentrée universitaire à l’ISVV et dont l’objectif sera de vérifier si d’autres molécules sont impliquées dans cette altération et de proposer des outils de diagnostic pour mesurer le risque d’apparition du goût de souris. A ce jour, les chercheurs ont mis en avant une corrélation entre la teneur en APY et l’intensité du goût de souris. Ainsi l’APY apparait comme un contributeur majeur et un bon marqueur de l’altération.
De nouvelles méthodes de dosage
Il existe un certains nombres de méthodes de dosage mais aucune n’est à ce jour officiellement validée. Certains laboratoires proposent un dosage par chromatographie en phase gazeuse associée à la spectrométrie de masse mais la méthode est longue (environ 5 jours) et coûteuse d’autant qu’elle ne permet pas le dosage simultanée des trois molécules. De nouvelles méthodes sont en cours de développement et utilise la chromatographie liquides (LC) : LC/Fluo (ISVV Bordeaux) ou LC-ES-MSMS (Laboratoire Excell). Ces méthodes permettent de s’affranchir des problèmes liés à la volatilité des composés, n’impliquant pas de modification du pH du vin avant analyse. La préparation de l’échantillon est donc plus rapide.
Pour en savoir plus :
https://techniloire.com/actualite/le-gout-de-souris-une-deviation-aromatique-encore-meconnue
Consultez aussi Tous les articles


Les adeptes de la vinification sans sulfite
Si les consommateurs exigent moins de sulfites dans leur vin, réduire les doses de SO2, principalement au niveau de la vinification avec la bio-protection, est aussi un moyen de retrouver de la typicité, apporter de la fraîcheur ou lutter contre les Brett.
"Dans dix ans, 80 % des vinifications se feront sans sulfite" déclare Arnaud Immélé, œnologue et auteur de l’ouvrage « Les grands vins sans sulfites », lors d’une table ronde sur le soufre à Chinon, organisée par le Syndicat des vins de Chinon le 6 septembre dernier. Après les rappels sur les actions antimicrobiennes et antioxydantes du soufre par la microbiologiste Joana Coulon, et la responsable technique Vinvention en Val-de-Loire Jenna Lebret, les échanges ont porté sur les moyens de vinifier sans sulfitage. « La réduction des sulfites ne doit pas uniquement répondre aux attentes des consommateurs, mais doit correspondre à la mise en œuvre de procédés technologiques pour obtenir de meilleurs vins », estime l’œnologue. Avec le sulfitage après récolte pratiqué habituellement, on ne sélectionne pas forcément les meilleures levures, et on participe à favoriser les Brettanomyces les plus résistantes. « Dès le départ, on crée une action sélective négative. Le sulfitage des jus suivi du levurage est le principal facteur de destruction de la typicité des vins », insiste Arnaud Immélé, pour qui la typicité des vins ne passe pas forcément par des souches de saccharomyces du domaine, notamment la réalisation de pied de cuve.
La vinification sans sulfite par la bio-protection
Cette technique consiste à protéger les jus de l’invasion microbiologique indésirable, en apportant des souches choisies, comme Primaflora constitué de souches non saccharomyces, qui colonisent le milieu et ne laissent pas de place à la flore indésirable telle que les Brettanomyces ou des bactéries lactiques productrices d’amines biogènes ou encore d’odeur butyriques et d’acétamide. « L’intérêt est d’appliquer la bio-protection le plus tôt possible dans le processus, au moment de la récolte, du pressurage ou de l’encuvage, à raison de 2 à 5 grammes/hl, soit l’équivalent des doses de SO2 », complète Arnaud Immélé, qui précise qu’il faut compter environ 100 euros/kg pour ces levures non saccharomyces. Pour Stéphane Yerle, vigneron à St Chinian et consultant, la bio-protection active offre divers avantages en jouant sur les capacités de certaines levures, notamment à apporter du gras aux rouges trop taniques (souche Torulaspora Delbrueckii), apporter de la fraîcheur par la production d’acides lactiques ou succiniques en phase pré-fermentaire par Pichia kluyverri ou Lachanceans thermotolerans, ou encore lutter contre les Brett par une stabilisation du milieu. « Il faut avoir confiance ! La bio-protection est aussi efficace que le sulfitage », continue Arnaud Immélé, qui précise cependant que son interdiction dans le cahier des charges Demeter la rend pour l’heure difficilement applicable en biodynamie. Pour l’élevage à l’inverse, se passer de soufre reste plus compliqué reconnait l’œnologue : « Ne plus utiliser de soufre en élevage demande beaucoup plus de technique et des équipements, afin de réduire les apports en oxygène jusqu’à l’embouteillage. »
Consultez aussi Tous les articles


Que sait-on de la contamination des vins par les phtalates et le bis-phénol A ?
A l’occasion du SITEVI 2015, Magali Grinbaum et Aurélie Camponovo de l’IFV ont présenté les résultats des travaux quant à l’impact des itinéraires techniques viti-vinicoles sur les teneurs en phtalates et bisphénol A provenant des matériaux en contact du vin. Ces travaux nationaux ont été réalisés en collaboration avec les interprofessions dont InterLoire. L’une des conclusions est que l’époxy reste la source la plus importante de contamination.
Les phtalates sont des composés chimiques dérivées de l’acide phtalique couramment utilisés comme plastifiants des matières plastiques, notamment du polychlorure de vinyle (PVC), quant au Bisphénol A (BPA), il entre dans la composition des plastiques et des résines époxydes. Ces composés sont des perturbateurs endocriniens toxiques pour la reproduction. Ils peuvent migrer dans le vin et le risque de migration varie selon 6 critères :
- La concentration de la substance dans le matériau
- Les propriétés chimiques du composé
- Le degré alcoolique du vin (substances très solubles dans l’alcool)
- La température et le temps de contact
- La géométrie de l’emballage
- La structure du matériau
Aucune réglementation sur leur présence dans les aliments
A ce jour, il existe dans la réglementation une liste positive des composés pouvant être présents dans la composition des matériaux au contact alimentaire. La réglementation définit aussi des restrictions et spécifications (Limite de Migration Spécifique ou LMS) propres à chaque molécule autorisée. Mais elles ne concernent que les matériaux, pas les aliments ni le vin. Ce flou réglementaire a été à l’origine des tensions avec la Chine en 2012-2013 liées au blocage de vins contenant des phtalates dans des doses supérieures aux LMS de la réglementation européenne. Quasiment pas de contamination avant la fermentation alcoolique L’objectif de l’étude nationale coordonnée par l’IFV a été d’acquérir des connaissances sur la présence de phtalates et de BPA dans les vins. Notamment d’évaluer l’impact des itinéraires techniques et d’identifier les origines des contaminations tout au long de la chaine d’élaboration, du raisin au conditionnement. Pour cela 383 vins issus de 50 itinéraires techniques différents ont été analysés entre 2012 et 2015. L’étude a porté sur 13 molécules (11 phtalates, le DBS ou dibutyl sebacate et le BPA). Les analyses sur moût montrent une très faible présence de phtalates et de BPA voire une absence de contamination : seuls 2 % des moûts contiennent quelques traces de ces composés. Les phtalates s’avèrent être les plus fréquemment retrouvés dont le DBP (dibutyl phtalate) relevés dans 50% des cas à une teneur moyenne de 48 μg/l (LMS de 300 μg/l). Le BPA n’a été retrouvé que dans 21% des cas à une teneur moyenne de 28 μg/l (LMS de 600 μg/l). Ceci s’explique par le fait qu’avant la fermentation alcoolique, les temps de contact sont faibles et il
n’y a pas encore d’alcool dans le milieu. Les conditions, à ce stade, ne favorisent pas la migration de ces composés dans le vin.
Des teneurs dans le vin très faibles, ne dépassant pas les LMS
L’analyse de 64 vins révèle une contamination par le DBP dans 45 % des cas, par le BBP (benzylbutylphtalate) dans 22% des cas et par le BPA dans 19 % des cas. Les contaminations se traduisent par des teneurs très faibles ne dépassant pas les LMS fixées par la réglementation. Les teneurs les plus élevées de DBP ont été retrouvées dans les vins stockées dans des cuves époxy. Les conditions d’élevage impactent également les teneurs en phtalates et BPA. L’élevage en bois ou inox n’engendre pas d’enrichissement en phtalates ou BPA quelle que soit la durée d’élevage. En revanche il y a une augmentation des teneurs en DBP durant un élevage en cuve époxy et en DMP (phtalate interdit) après 18 mois d’élevage en cuve de fibre de verre. L’analyse de 119 vins mis en bouteilles montre la présence de DBP dans 63% des cas, et de BPA dans 29 % des cas. Ces teneurs augmentent après plusieurs mois de conditionnement. Il semble donc que le matériel de mise en bouteilles et/ou les conditions de stockage des bouteilles sèches (film plastique) soient source de contamination.
Baisse des teneurs en phtalates dans les BIB
Dans les 40 BIB analysés, le DBP a été majoritairement retrouvé. Néanmoins entre les prélèvements effectués avant conditionnement et après plusieurs mois de conditionnement, une baisse de la teneur en DBP est observée. Il semble qu’il y ait un phénomène d’adsorption des molécules par le polyéthylène constitutif des BIB. Il serait intéressant d’approfondir cette hypothèse en étudiant plus précisément l’impact des caractéristiques techniques des poches (épaisseur, contenance, polyéthylène,…). Une autre étude menée dans le Beaujolais comparant les BIB, les bouteilles en verre et les PET ne met pas en avant d’enrichissement des vins en phtalates via ce conditionnement. Enfin des travaux sur différents bouchons synthétiques conduits en Alsace montrent qu’il n’y a pas d’incidence de l’obturateur sur la teneur en phtalates.
Focus sur les résines époxy
Il est montré que le revêtement époxy des cuves est à l’origine de plus grands risques de migration, notamment si les conditions d’application ne sont pas respectées ou la polymérisation s’est mal faite. Voici quelques précautions énoncées par Aurélie Camponovo de l’IFV :
- Demander la documentation de la fabrication de la résine et les certificats de l’applicateur
- Comparer les devis
- Entretenir les cuves
- Contrôler la teneur en phtalates des vins : LMS et respect de la DJA (dose journalière autorisée)
Consultez aussi Tous les articles


Le goût de souris, une déviation aromatique encore méconnue
Le goût de souris est une déviation organoleptique qui suggère des odeurs de souris, pop corn, tortilla etc… Souvent méconnue, cette déviation n'en reste pas moins préoccupante car non prévisible... Nicolas Richard, ingénieur oenologue du service R&D d'Inter-Rhône présente quelques pistes de réflexions pour mieux appréhender cette finale aromatique souvent sournoise.
D’où vient le goût de souris ?
Nicolas Richard : La recherche aujourd’hui a démontré que deux microorganismes, les levures Brettanomyces et les bactéries lactiques Lactobacillus et Oenococcus sont à l’origine de ces déviations. À partir de deux acides aminés, la lysine et l’ornithrine, trois molécules sont synthétisées : le 2 acétyltétrahyropyridine ATHP, le 2 éthyltétrahydropyridine et le 2 acétyl 1 pyroline. Selon de récentes études, il existerait une autre voie de synthèse. D’autres molécules pourraient ainsi être synthétisées, peut être des pyridines… Les deux types de microorganismes peuvent intervenir sans la présence de l’autre. Lorsqu’il y a synthèse d’ATHP, cette déviation se manifeste lorsque le pH augmente et l’acidité diminue. En bouche, la salive a tendance à augmenter le pH de la solution. Il semblerait qu’à pH élevé, un isomère des molécules responsables du goût de souris passe sous une autre forme chimique qui serait détectée par l’homme.
Comment détecter un goût de souris ?
Nicolas Richard : Tous les dégustateurs ne sont pas égaux puisque le pH de la salive agit sur la perception du défaut. Or le pH varie d’un individu à l’autre voire le pH salivaire d'un même individu varie au cours de la journée ! Si vous mangez des huîtres avec du jus de citron vous ne sentirez pas cette déviation ! Les odeurs associées sont : souris, tortilla, peau de saucisson, voire vomi dans certains cas et eau du riz basmati. Les molécules responsables de l’odeur de l’eau du riz basmati, à base de pyridines, sont bien connues parce qu’étudiées par l’industrie agroalimentaire. Deux essais peuvent être réalisés pour révéler la présence d’ATHP. Pour en être certain vous pouvez tremper le doigt dans le vin, attendre quelques secondes et sentir… le pH de la peau augmente celui du vin et l’odeur peut ainsi être perçue par l’homme. Autre astuce imparable : mettre une cuillère de bicarbonate de soude dans un verre du vin suspect. Il y aura une effervescence et un dégagement de l’odeur instantanément.
Quelles sont les solutions curatives ?
Nicolas Richard : Les vins sulfités à plus de 15 mg/l de SO2 libre ne sont pas affectés par cette déviation. L’anhydride sulfureux dès 2 g/hl diminue le goût, mais 5 g/hl ne le masquera pas plus. Il est ainsi inutile d’augmenter démesurément les doses de SO2. De mon côté, j’ai testé de nombreuses colles et j’ai obtenu une efficacité avec les tanins oenologiques : les ellagitanins à des doses de 5g/hl. Est-ce l’effet antioxydant des tanins qui agit ? Est-ce que les tanins masquent cette aromatique ? Autant de questions actuellement sans réponse. Il semble que ces molécules soient passagères. Les vignerons voient ce phénomène disparaître au bout de quelques mois. Surprenant mais rassurant. Si le vin est déjà en bouteille, il vaut mieux attendre… mais impossible de définir une durée. Ce goût serait probablement lié au potentiel redox du vin qui a tendance à varier avec le temps.
Quelles pourraient-être les mesures préventives ?
Nicolas Richard : Il faut respecter toutes les règles de préconisations d’un point de vue microbiologique, de l’hygiène en cave, et de la maîtrise des fermentations malolactiques… Si cette déviation apparaît pendant la fermentation alcoolique, elle a tendance à disparaître pendant la vinification.









